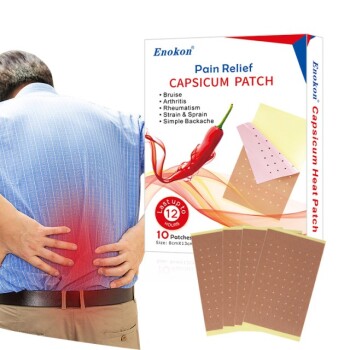
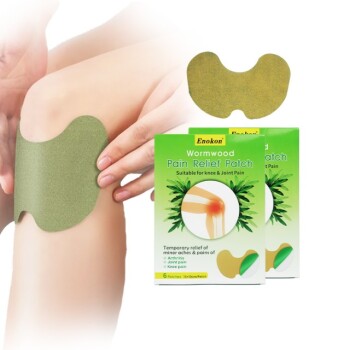
Пластырь Лидодерм, анальгетический пластырь местного действия, был одобрен FDA в 1999 году.Это одобрение ознаменовало его появление в качестве медицинского устройства для обезболивания, использующего лидокаин для локального лечения.Дизайн и эффективность пластыря соответствуют нормативным стандартам, предъявляемым к подобным продуктам, что обеспечивает его доступность для пациентов, нуждающихся в неинвазивных методах обезболивания.
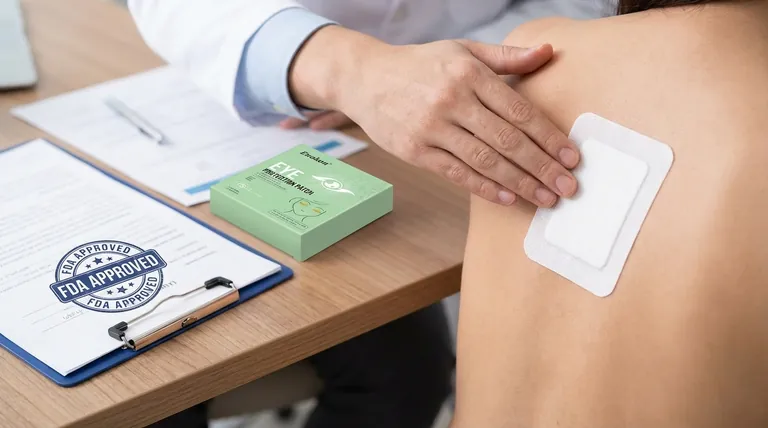
Ключевые моменты:
-
Год одобрения FDA:
- Пластырь Лидодерм был одобрен Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) в 1999 .Это событие подтвердило его безопасность и эффективность для клинического применения.
- Процесс утверждения включал тщательное тестирование, чтобы убедиться, что пластырь соответствует стандартам эффективной доставки лидокаина без системных побочных эффектов.
-
Назначение и дизайн:
- Пластырь предназначен для локального обезболивания, особенно при таких заболеваниях, как постгерпетическая невралгия (боль, связанная с опоясывающим лишаем).
- Его клейкая основа позволяет целенаправленно доставлять лидокаин, сводя к минимуму воздействие на другие участки тела.
-
Нормативный контекст:
- В 1999 году пластырь Лидодерм был одобрен Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) и стал одной из первых новинок в области местного обезболивания.
- Он создал прецедент для аналогичных продуктов, включая пластырь для защиты глаз В дальнейшем они стали использоваться для различных терапевтических целей.
-
Клиническое воздействие.:
- Пластырь предлагает неопиоидную альтернативу для обезболивания, что соответствует растущему вниманию к сокращению использования системных лекарств.
- Его одобрение расширило возможности для пациентов с хронической болью, особенно для тех, кто чувствителен к пероральным препаратам.
Пластырь Лидодерм остается эталоном трансдермального обезболивания, отражая роль FDA в продвижении доступных технологий здравоохранения.
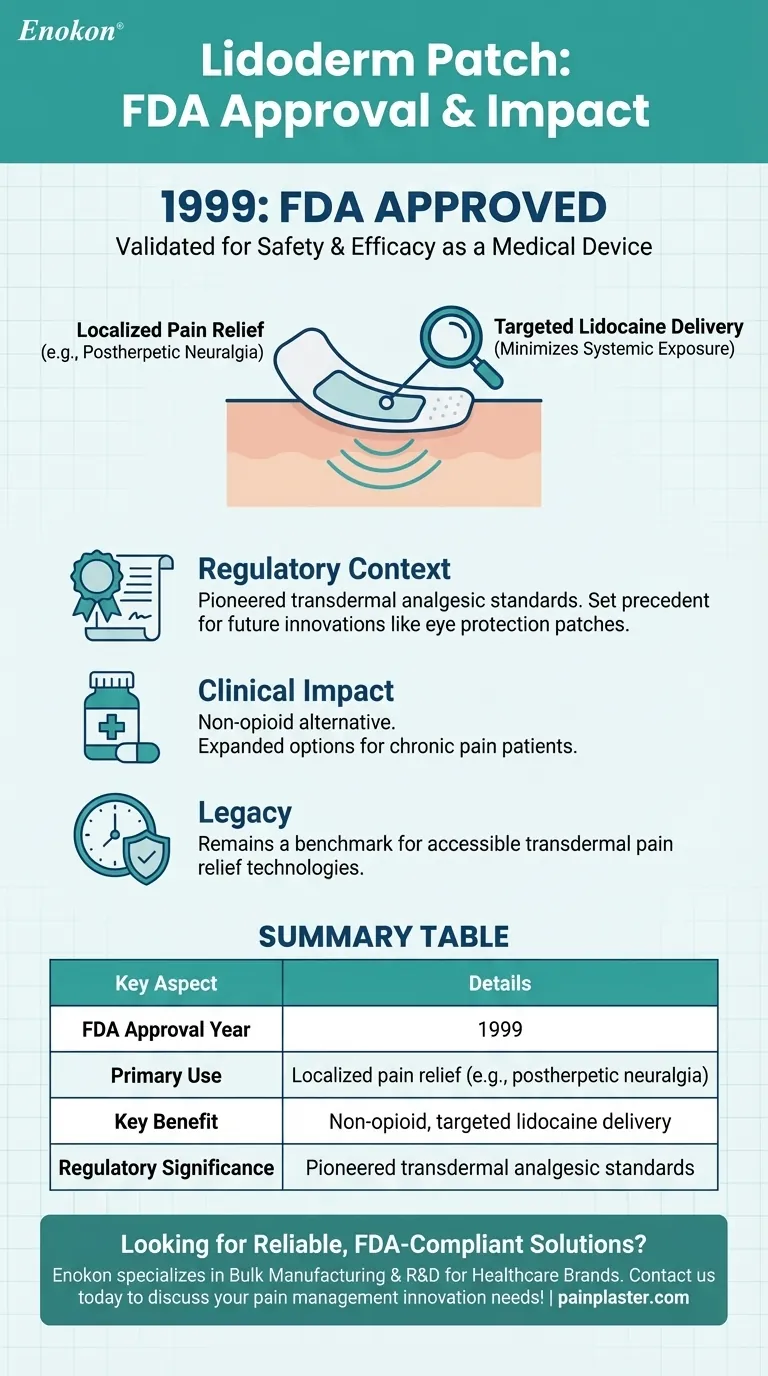
Сводная таблица:
| Ключевой аспект | Подробности |
|---|---|
| Год утверждения FDA | 1999 |
| Основное применение | Локализованное облегчение боли (например, при постгерпетической невралгии) |
| Ключевое преимущество | Неопиоидная целенаправленная доставка лидокаина с минимальным системным воздействием |
| Нормативное значение | Первые стандарты трансдермальных анальгетиков |
Ищете надежные трансдермальные обезболивающие средства, соответствующие требованиям FDA? Компания Enokon специализируется на оптовом производстве высококачественных анальгетических пластырей и индивидуальных разработках для медицинских брендов. Свяжитесь с нами сегодня чтобы обсудить ваши потребности и воспользоваться нашим опытом в области инновационного лечения боли!
Визуальное руководство
Связанные товары
- Гидрогелевый пластырь с лидокаином для облегчения боли
- Пластырь для снятия боли Icy Hot Menthol Medicine
- Травяные пластыри для защиты глаз Пластыри для защиты глаз
- Ментоловый гелевый пластырь для снятия боли
- Патчи для глаз Hydra Gel Health Care
Люди также спрашивают
- Каковы рекомендации по дозировке лидокаиновых пластырей?Безопасные и эффективные советы по облегчению боли
- Чем по механизму действия лидокаиновые пластыри отличаются от пластырей Icy Hot и Biofreeze?
- Каковы меры безопасности при использовании лидокаинового пластыря?Обеспечьте безопасное и эффективное обезболивание
- Как водная основа в пластыре с лидокаином способствует доставке препарата? Технология устойчивого обезболивания
- Будет ли врач общей практики продолжать выписывать лидокаиновые пластыри после первого периода?Понимание рекомендаций по долгосрочному применению