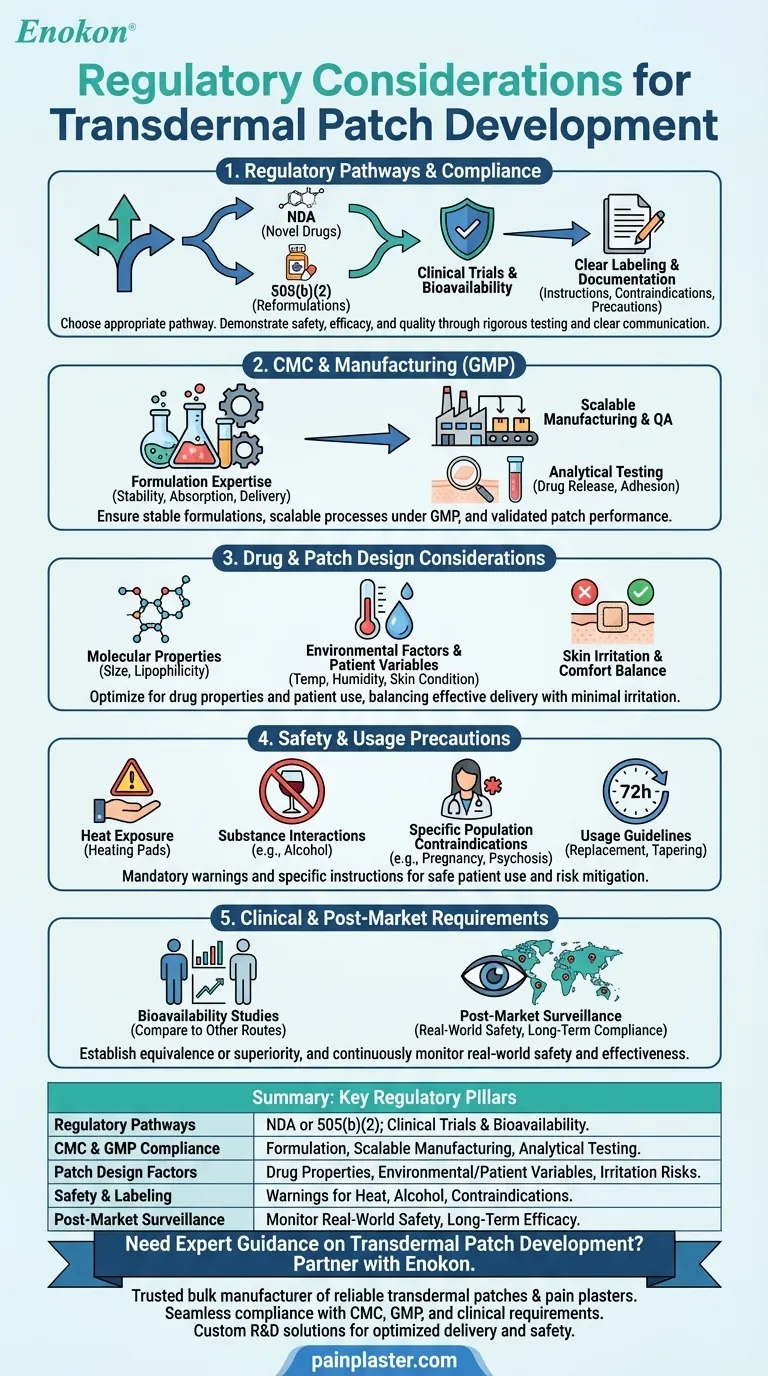
Разработка трансдермальных пластырей связана со сложной нормативно-правовой базой, обеспечивающей безопасность, эффективность и качество.Ключевыми моментами являются соблюдение требований к химии, производству и контролю (CMC), следование надлежащей производственной практике (GMP), а также тщательное клиническое тестирование на предмет биодоступности и безопасности.Дизайн пластыря должен учитывать свойства препарата (например, размер молекулы, полярность) и факторы окружающей среды, а маркировка и документация должны соответствовать строгим стандартам.В зависимости от новизны препарата могут применяться такие пути регулирования, как NDA или 505(b)(2).Для получения разрешения и обеспечения безопасности пациентов необходимо также учесть такие меры предосторожности, как риск раздражения кожи и ограничения по применению (например, избегать теплового воздействия).

Разъяснение ключевых моментов:
-
Пути регулирования и соблюдение требований
- Спонсорам приходится выбирать между подачей заявки на новый препарат (NDA) для новых лекарственных средств и путем 505(b)(2) для реформулирования одобренных препаратов.
- Соответствие трансдермальные пластыри Для получения разрешения на использование трансдермальных пластырей необходимо подтвердить безопасность, эффективность и качество с помощью клинических испытаний, включая исследования биодоступности.
- Обязательно наличие четкой маркировки и документации с подробным описанием инструкций по применению, противопоказаний (например, психоз, связанный с деменцией) и мер предосторожности (например, отказ от алкоголя или теплового воздействия).
-
Химия, производство и контроль (CMC)
- Для обеспечения стабильности, абсорбции и стабильной скорости доставки лекарственных средств очень важна экспертиза рецептур.
- Масштабируемость и обеспечение качества при коммерческом производстве должны соответствовать стандартам GMP.
- Аналитические испытания подтверждают эффективность пластырей, включая профили высвобождения лекарств и адгезивные свойства.
-
Особенности разработки лекарственных средств и пластырей
- Молекулярные свойства (например, малый размер, липофильность) влияют на скорость абсорбции и должны быть оптимизированы в процессе разработки.
- Факторы окружающей среды (температура, влажность) и специфические для пациента переменные (состояние кожи, возраст) влияют на эффективность и требуют тестирования в реальных условиях.
- Пластыри должны обеспечивать баланс между доставкой лекарств и комфортом, сводя к минимуму раздражение кожи или аллергические реакции.
-
Меры безопасности и предосторожности при использовании
- Маркировка должна предупреждать о таких рисках, как раздражение кожи, тепловое воздействие (например, грелки) и взаимодействие с такими веществами, как алкоголь.
- Для особых групп населения (беременные/кормящие, больные психозом) могут потребоваться противопоказания.
- Рекомендации по применению (например, замена каждые 72 часа, протоколы снижения дозы) должны быть четко доведены до сведения пациентов.
-
Клинические и постмаркетинговые требования
- Исследования биодоступности сравнивают трансдермальную доставку с другими способами (например, пероральным), чтобы установить эквивалентность или превосходство.
- Постмаркетинговое наблюдение контролирует безопасность в реальном мире, обеспечивая долгосрочное соблюдение требований и устраняя непредвиденные побочные эффекты.
Учет этих аспектов позволяет разработчикам преодолевать нормативные препятствия и одновременно создавать эффективные трансдермальные препараты, удобные для пациентов.Задумывались ли вы о том, как могут измениться клеи для пластырей, чтобы уменьшить раздражение кожи без ущерба для доставки лекарств?
Сводная таблица:
| Основные нормативные аспекты | Подробности |
|---|---|
| Пути регулирования | NDA для новых препаратов; 505(b)(2) для реформулирующих препаратов.Требуются клинические испытания и исследования биодоступности. |
| Соответствие требованиям CMC и GMP | Стабильность рецептуры, масштабируемое производство и аналитические испытания (высвобождение препарата, адгезия). |
| Факторы дизайна пластыря | Оптимизация свойств препарата (размер, липофильность), переменных окружающей среды/пациента и риска раздражения кожи. |
| Безопасность и маркировка | Предупреждение о вреде теплового воздействия, взаимодействии с алкоголем и противопоказаниях для групп повышенного риска. |
| Постмаркетинговое наблюдение | Отслеживайте безопасность в реальном мире и долгосрочную эффективность после утверждения. |
Нужны экспертные рекомендации по разработке трансдермальных пластырей? Сотрудничайте с Энокон надежный производитель надежных трансдермальных пластырей и обезболивающих пластырей для медицинских брендов и дистрибьюторов.Наш технический опыт обеспечивает беспрепятственное соблюдение требований CMC, GMP и клинических испытаний, а наши индивидуальные решения в области исследований и разработок оптимизируют доставку лекарств и безопасность пациентов. Свяжитесь с нами сегодня чтобы обсудить ваш проект!
Визуальное руководство
Связанные товары
- Трансдермальные пластыри с дальним инфракрасным теплом для облегчения боли
- Силиконовые пластыри от шрамов Трансдермальный лекарственный пластырь
- Пластырь для снятия боли Icy Hot Menthol Medicine
- Ментоловый гелевый пластырь для снятия боли
- Пластырь для снятия боли в шее с полынью
Люди также спрашивают
- Каково назначение вакуумной фильтрации для полимерных растворов? Обеспечение качества при производстве трансдермальных пластырей
- Какие факторы влияют на эффективность трансдермальных пластырей?Ключевые аспекты оптимальной доставки лекарств
- Какие клинические преимущества дают трансдермальные пластыри пожилым пациентам?Оптимизируйте гериатрический уход с легкостью
- Каковы недостатки трансдермальной доставки лекарств?Основные ограничения, которые необходимо учитывать
- Какую роль играют трансдермальные пластыри в улучшении состояния кожных поражений? Узнайте, как стабилизация предотвращает пролежни