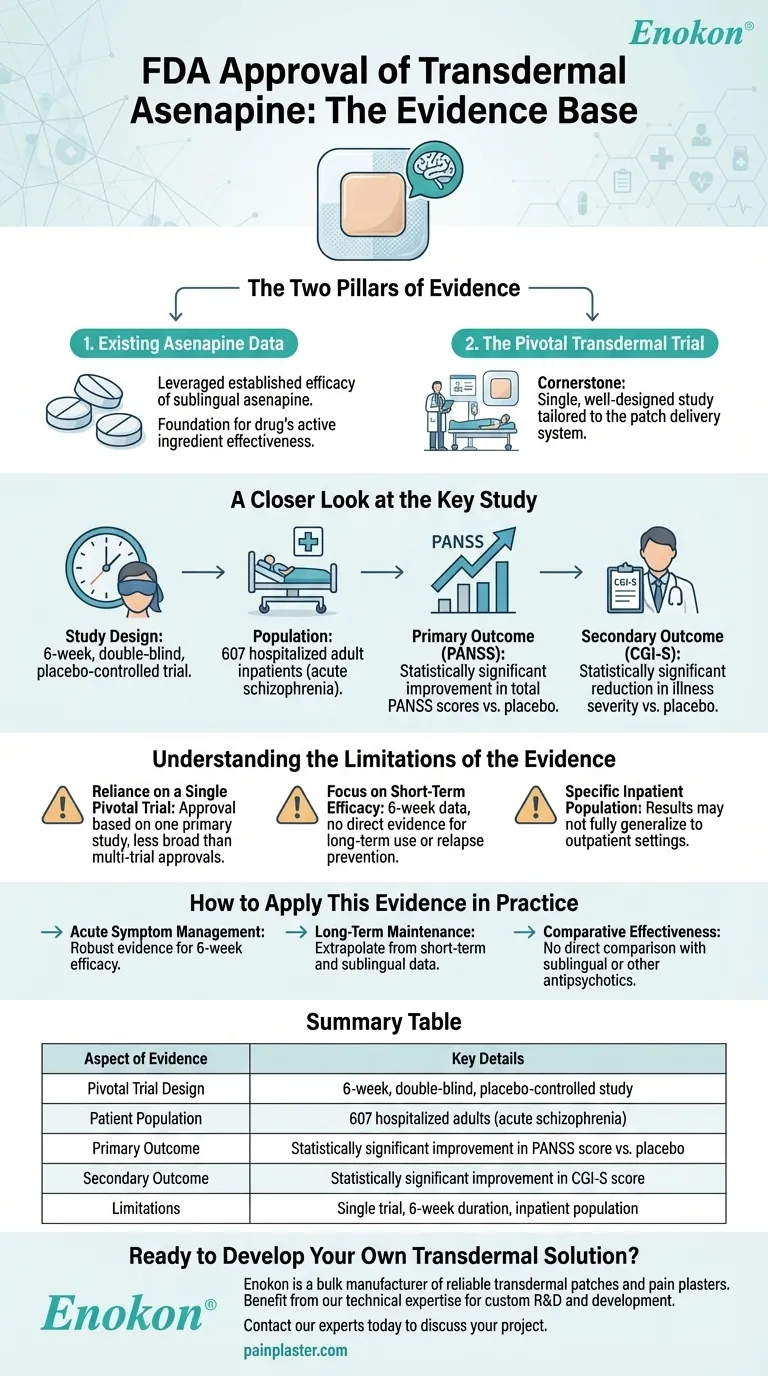
FDA одобрило пластырь с асенапином (трансдермальный асенапин) был создан на основе совокупности предыдущих данных об эффективности сублингвального асенапина и результатов основного 6-недельного двойного слепого плацебо-контролируемого исследования с участием 607 взрослых стационарных пациентов с шизофренией.Трансдермальный препарат продемонстрировал статистически значимое улучшение как первичных (оценка по шкале PANSS), так и вторичных (оценка по шкале CGI-S) конечных точек по сравнению с плацебо, что подтверждает его терапевтическую пользу.Эти данные в совокупности подтвердили безопасность, эффективность и клиническую значимость пластыря для лечения шизофрении.
Ключевые моменты разъяснены:
-
Предыдущие данные об эффективности сублингвального асенапина
- Предыдущие испытания сублингвального асенапина позволили получить фундаментальные данные о механизме действия препарата и его терапевтическом потенциале при шизофрении.
- Эти исследования, вероятно, позволили определить дозировку, профили безопасности и ожидаемые результаты для трансдермального препарата, что упростило путь к одобрению.
-
Пивотальное 6-недельное двойное слепое исследование
- Дизайн исследования:Строгое плацебо-контролируемое исследование с 607 участниками обеспечило надежную статистическую мощность и минимизировало смещение.
- Население:Ориентирован на взрослых стационарных пациентов с шизофренией, что отражает целевую демографическую группу для клинического использования.
- Продолжительность:6-недельные сроки сбалансировали оценку острых симптомов и практическую клиническую применимость.
-
Первичная конечная точка:баллы по шкале PANSS
- Шкала позитивного и негативного синдрома (PANSS) является золотым стандартом для оценки тяжести симптомов шизофрении.
- Статистически значимое улучшение показателей по PANSS подтвердило эффективность пластыря в снижении как позитивных (например, галлюцинаций), так и негативных (например, социальной замкнутости) симптомов.
-
Вторичная конечная точка:Оценки по шкале CGI-S
- Шкала глобального клинического впечатления-тяжести (CGI-S) обеспечила подтверждение улучшения симптомов по отзывам врачей.
- Значимость в данном случае усиливалась специфическими для пациента и наблюдаемыми клиническими преимуществами.
-
Безопасность и переносимость
- Несмотря на то, что в рекомендациях нет четкого описания, одобрение FDA подразумевает, что трансдермальная формула соответствует стандартам безопасности, вероятно, на основе данных о сублингвальном применении и новых отчетах о неблагоприятных событиях.
- Трансдермальная доставка может иметь такие преимущества, как снижение системных побочных эффектов (например, по сравнению с пероральным или инъекционным способом).
-
Нормативное обоснование
- Решение FDA основывалось на воспроизводимой эффективности (PANSS/CGI-S) и четком профиле риск-польза, подтвержденном данными контролируемых исследований.
- Удобство применения пластыря и его преимущества (например, устойчивое высвобождение, неоральный способ применения) могли еще больше обосновать одобрение для населения, которое часто испытывает трудности с соблюдением режима приема лекарств.
Для закупщиков медицинских услуг эти данные подчеркивают, что пластырь с асенапином как жизнеспособный, подтвержденный доказательствами вариант лечения шизофрении, обладающий потенциальными преимуществами в применении и переносимости.Соответствует ли его трансдермальный формат потребностям ваших пациентов или институциональным протоколам?
Сводная таблица:
| Основные доказательства для одобрения FDA | Подробности |
|---|---|
| Предварительные данные о сублингвальном асенапине | Установленный механизм действия и профиль безопасности |
| Поворотное 6-недельное исследование | 607 взрослых стационарных пациентов с шизофренией, двойное слепое, плацебо-контролируемое исследование |
| Первичная конечная точка (баллы по шкале PANSS) | Статистически значимое уменьшение симптомов |
| Вторичная конечная точка (оценки по шкале CGI-S) | Подтвержденное врачом улучшение тяжести заболевания |
| Безопасность и переносимость | Соответствует стандартам FDA, потенциальные преимущества в отношении приверженности к лечению |
| Нормативное обоснование | Воспроизводимая эффективность и четкий профиль риск-польза |
Заинтересованы в интеграции трансдермального асенапина в ваши протоколы лечения?
Являясь надежным оптовым производителем трансдермальных пластырей и обезболивающих пластырей, Энокон предлагает надежные, клинически проверенные решения для дистрибьюторов медицинских услуг и фармацевтических брендов.Наш опыт в области индивидуальных исследований и разработок гарантирует создание рецептур, отвечающих потребностям ваших пациентов.
Свяжитесь с нами сегодня чтобы обсудить возможности сотрудничества или запросить образцы продукции.
Визуальное руководство
Связанные товары
- Силиконовые пластыри от шрамов Трансдермальный лекарственный пластырь
- Трансдермальные пластыри с дальним инфракрасным теплом для облегчения боли
- Ментоловый гелевый пластырь для снятия боли
- Пластырь для снятия боли Icy Hot Menthol Medicine
- Пластырь для снятия боли в шее с полынью
Люди также спрашивают
- В чем преимущества трансдермальных лекарственных пластырей?Оптимизируйте доставку лекарств с помощью пластырей
- Как трансдермальные пластыри используются в лечении психических заболеваний? Преимущества и применение
- В чем заключаются основные преимущества трансдермальных систем доставки лекарств?Повышение эффективности лечения благодаря точности и удобству
- Как состояние кожи, возраст и окружающая среда влияют на эффективность трансдермальных пластырей?Оптимизируйте доставку лекарств
- Какую роль играет система трансдермальной доставки на основе силикона при болезни Паркинсона? Улучшение ухода за пациентами на ранней стадии











