Трансдермальный клонидин был первоначально одобрен Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) в 1984 году для лечения гипертонии легкой и умеренной степени, как самостоятельный препарат или в комбинации с диуретиком.Это одобрение ознаменовало появление нового способа доставки клонидина, использующего его способность снижать артериальное давление за счет механизмов центрального альфа-агониста.Трансдермальный пластырь обладал такими преимуществами, как устойчивое высвобождение препарата и улучшенная комплаентность пациентов, что на тот момент было значительным достижением в лечении гипертонии.
Ключевые моменты:
-
Первоначальное одобрение FDA (1984 год)
- Трансдермальный клонидиновый пластырь был одобрен FDA в 1984 году специально для лечения гипертонии легкой и умеренной степени.
- Это разрешение подтвердило его эффективность в качестве монотерапии или дополнения к диуретикам, что позволило удовлетворить острую потребность в антигипертензивных средствах длительного действия.
-
Основное показание:Гипертония
-
Пластырь был разработан для обеспечения непрерывной доставки клонидина, снижающего артериальное давление за счет:
- Снижения частоты сердечных сокращений.
- Расслабляет кровеносные сосуды, улучшая кровообращение.
- Его классификация как альфа-агонист центрального действия, гипотензивный препарат подчеркивает механизм его действия в стволе мозга для модуляции симпатического оттока.
-
Пластырь был разработан для обеспечения непрерывной доставки клонидина, снижающего артериальное давление за счет:
-
Преимущества трансдермальной доставки
- В отличие от пероральных препаратов, пластырь обеспечивает стабильный уровень препарата, сводя к минимуму колебания между пиком и впадиной.
- Снижение частоты дозирования (например, еженедельное применение) повышает приверженность к лечению, особенно при хронических заболеваниях, таких как гипертония.
-
Возрастные ограничения
- Примечательно, что трансдермальная форма препарата не была одобрена для пациентов младше 18 лет, что отражает ограниченные данные по безопасности в педиатрической популяции на тот момент.
-
Исторический контекст
- Одобрение 1984 года стало инновацией в области доставки лекарств, что соответствует более широким тенденциям, связанным с непероральными методами лечения сердечно-сосудистых заболеваний.
- Он дополнял существующий пероральный клонидин, предлагая альтернативу для пациентов с проблемами переносимости желудочно-кишечного тракта.
Трансдермальный пластырь с клонидином остается свидетельством того, как системы адресной доставки лекарств могут изменить лечение хронических заболеваний, спокойно оптимизируя терапию благодаря научному подходу.
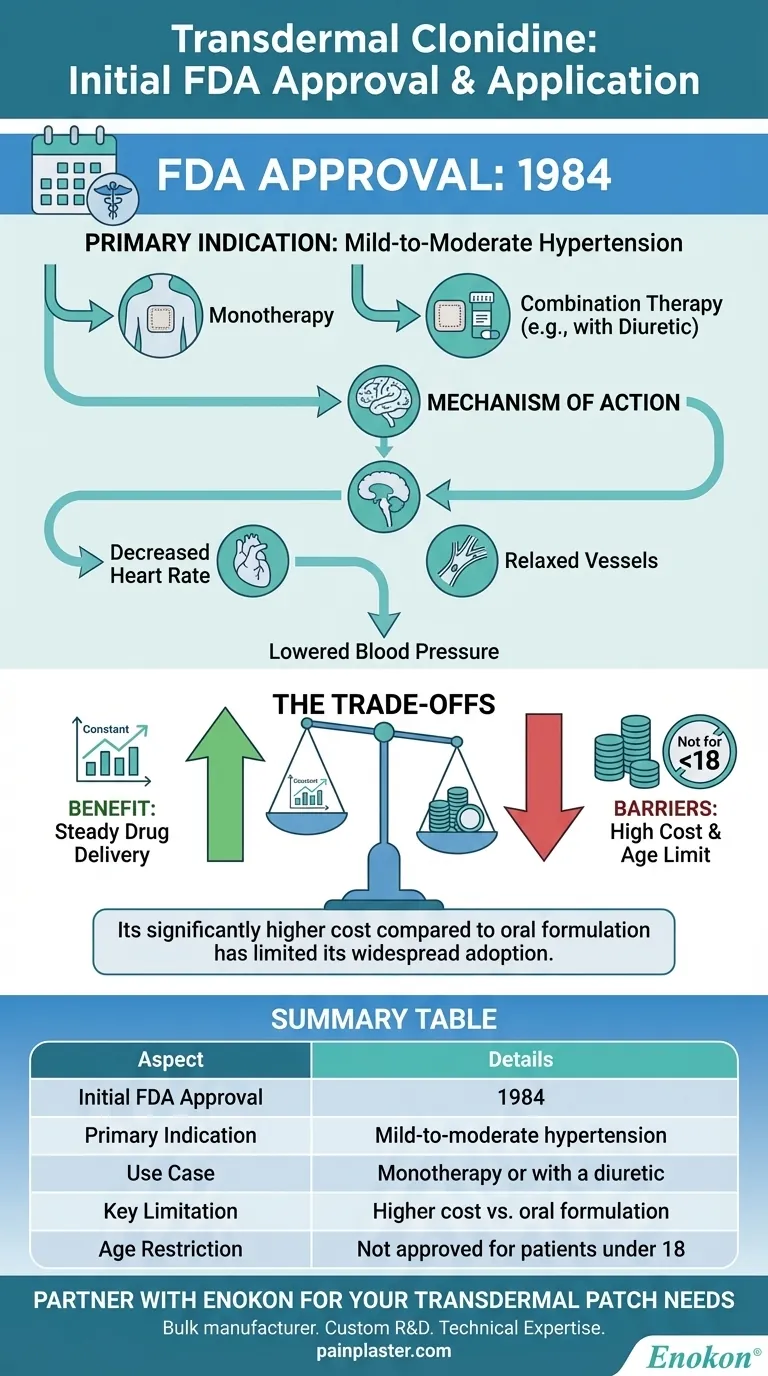
Сводная таблица:
| Ключевой аспект | Подробности |
|---|---|
| Год утверждения FDA | 1984 |
| Основное показание | Гипертония легкой и умеренной степени (монотерапия или вместе с диуретиками) |
| Механизм действия | Альфа-агонист центрального действия, снижает симпатический отток |
| Ключевые преимущества | Постоянное высвобождение препарата, улучшенное соблюдение режима, еженедельное дозирование |
| Возрастные ограничения | Не одобрено для пациентов младше 18 лет |
Нужны надежные трансдермальные решения для лечения гипертонии или хронической боли?
Компания Enokon специализируется на высококачественных трансдермальных пластырях, сочетая десятилетия опыта с индивидуальными исследованиями и разработками для фармацевтических брендов и дистрибьюторов.
Свяжитесь с нами сегодня
чтобы обсудить ваш проект - давайте внедрять инновации вместе!
Визуальное руководство
Связанные товары
- Ментоловый гелевый пластырь для снятия боли
- Силиконовые пластыри от шрамов Трансдермальный лекарственный пластырь
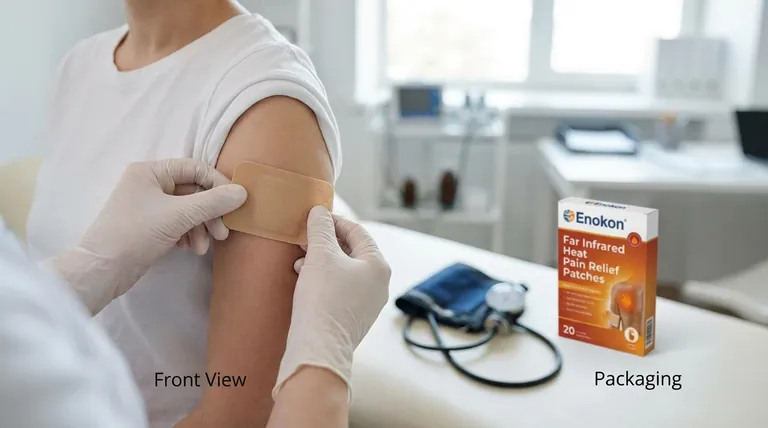
- Трансдермальные пластыри с дальним инфракрасным теплом для облегчения боли
- Пластырь для снятия боли Icy Hot Menthol Medicine
- Пластырь для снятия боли в шее с полынью
Люди также спрашивают
- Когда стоит задуматься об использовании обезболивающих средств, таких как кремы и пластыри?Оптимизация комфорта и безопасности
- Как часто применяются обезболивающие пластыри?Целенаправленное облегчение боли
- Каковы возможные побочные эффекты обезболивающих пластырей?Риски и советы по безопасности
- Чем обезболивающие пластыри отличаются от других методов облегчения боли?Откройте для себя целенаправленное и длительное облегчение
- Что такое обезболивающие пластыри и как они работают?Откройте для себя неинвазивные методы лечения боли




